Pfizers „Pax Rovid“ wird weltweit entwickelt . Aber in gewisser Weise ist es experimenteller als die Covid-Injektion des Unternehmens . Health Canada zum Beispiel steht seit Jahrzehnten auf der Seite von Pharmaunternehmen wie der US-amerikanischen FDA, aber „nicht viele Menschen haben Paxrovid eingenommen. Es kann schwerwiegende und unerwartete Nebenwirkungen haben. “ Ich gebe es zu.
Ein riesiger Lastwagen rollt in Richtung Ottawa, begleitet von zahlreichen Unterstützern und Medienberichten.
In der Zwischenzeit beginnt Paxrovid von Pfizer relativ ruhig in Nordamerika, Europa, Großbritannien und anderswo auf den Markt zu kommen.
Dies ist ein Medikament für COVID und der zweite Doppelschlag, der mit der mRNA – COVID-Injektion des Unternehmens begann .
Gemeinsam erzielt Pfizer spektakuläre Gewinne und Marktkapitalisierung .
Es ist jedoch unwahrscheinlich, dass das Medikament „Pax“ (lateinisch für Frieden) ergibt.
Paxlobid wurde bisher an einer sehr kleinen Anzahl von Menschen getestet. Es wurden keine Studien an geimpften oder COVID-infizierten Personen durchgeführt. Dieses Arzneimittel hat eine negative Wirkung auf viele der am häufigsten verwendeten Arzneimittel. Darüber hinaus wird die Forschung natürlich manipuliert, um scheinbar gute Ergebnisse zu liefern.
Ich habe gehört, dass einige Aufsichtsbehörden es leid sind, dem starken Druck von Politikern, Gesundheitsbehörden und großen Pharmaunternehmen nachzugeben. Sie wollen nicht, dass die breite Öffentlichkeit Medikamente einnimmt, die in dieser äußerst unzureichenden Studie potenziell extrem gefährlich sein können.Eine Einzeldosis Paxroid besteht aus einem wiederverwendbaren alten HIV-Medikament, Ritonavir , und zwei neuen Medikamenten, Nirmatorelvir . Beide Medikamente sind Protease-Inhibitoren.
Diese Kombinationstherapie aus Nirmatolvir und Ritonavir wurde von der Food and Drug Administration (EUA) am 22. Dezember 2021 in den Vereinigten Staaten und von Health Canada Kanadaam 17. Januar 2022 in
Darüber hinaus nimmt die Zulassung in anderen Ländern rapide zu, beispielsweise die Zulassung am Frankreich2022 inJanuarVereinigten Königreich und2021 im31. Dezember,Südkorea202127. Dezemberam,Israel26. Dezember 2021 in
In den Vereinigten Staaten, Israel und Südkorea ist es für Jugendliche und Erwachsene über 12 Jahren zugelassen. In anderen Ländern wie dem Vereinigten Königreich und Kanada sind Personen über 18 Jahren berechtigt.
(Genehmigung ist nicht Genehmigung, sie wurde nach einer sehr schnellen Bewertung von zig Millionen Menschen genehmigt.)
Darüber hinaus haben Tests von Pfizer-Wissenschaftlern an Petrischalen gezeigt, dass sie einige Auswirkungen auf die Omicron–Canada- Spezifikation vom 22. Januar Auf der Grundlage dieser sehr dünnen Beweise berichten die Mainstream-Medien ausführlich, dass „dieses Medikament voraussichtlich gegen Omicron wirksam sein wird“.
Nermatrelvir / Ritonavir- Tabletten sind für die Verwendung durch Personen zugelassen, die positiv auf Covid getestet wurden, leichte oder mittelschwere Symptome haben und ein „hohes Risiko haben, eine schwere COVID-19 zu entwickeln“.
Aber wie definiert Pfizer ein hohes Risiko?
Muss über 60 Jahre alt sein. Oder Übergewicht. Bluthochdruck. Oder viele andere Dinge – einschließlich „anderer Zustände oder Faktoren (z. B. Rasse oder ethnische Zugehörigkeit), die den Patienten einem hohen Progressionsrisiko aussetzen können“. (Siehe Seite 8 der Spezifikation vom 22. Januar in Kanada )
Dies ist eine sehr weit gefasste Definition.
Eine weitere alarmierende Tatsache ist, dass die Vereinigten Staaten und Kanada entschieden haben, Nirmatrelville / Ritonavir ausschließlich auf der Grundlage der Zwischenanalyse laufender Studien zuzulassen. Die Prüfung beginnt am 25. August 2021 und endet etwa am 24. April 2022 .Als Nilmatrelvir/Ritonavir von den US-amerikanischen und kanadischen Behörden genehmigt wurde , war insgesamt etwa 1.000 Personen Nirmatrelvir/Ritonavir nach dem Zufallsprinzip verabreicht worden.
(Es ist sehr schwierig, die konkreten Zahlen zu entschlüsseln. Pfizers Pressemitteilung vom 5. November 2021 , in der die von der FDA untersuchte Zwischenanalyse beschrieben wird, und die kanadische Produktmonographie vom 17. Januar 2022 (etwas später). Es gibt eine Reihe von Zahlen und einige Arten der Datenanalyse, die beide am selben Tag analysiert werden). Außerdem waren nur 13 % der Minderheit 65 Jahre oder älter und nur 3 % waren 75 Jahre oder älter. ( Siehe Abschnitt 1.2 mit dem Titel „Alter“ auf Seite 4 der Paxrovid-Produktmonographie, veröffentlicht in Kanada am 17. Januar 2022 ).
Zudem wurden auch solche Zwischenergebnisse im Testbericht maximal manipuliert (dazu später mehr). In den Vereinigten Staaten war die Pressemitteilung von Pfizer einfach der 5. November 2021 .

Außerdem hat Pfizer die Originaldaten, die Health Canada zur Verfügung gestellt wurden, soweit ich das finden konnte, nicht offengelegt. Darüber hinaus enthielt die Pressemitteilung des Unternehmens zur Zulassung in Kanada vom 17. Januar 2022 nur sehr wenige Details.
Es war alles sehr vorhersehbar.
Das heißt, am 18. November 2021, mehr als einen Monat vor der FDA-Zulassung, unterzeichnete die US-Regierung einen von der FDA genehmigten Nirmatrelville / Ritonavir 10-Millionen-Kurs (530 US-Dollar pro Kurs) für 5,3 Milliarden US-Dollar.
In ähnlicher Weise gab die kanadische Regierung am 3. Dezember 2021 eine Zusage zum Kauf von Nirmatreville / Ritonavir von Pfizer für zunächst 1 Million Kurse bekannt, in Erwartung der Genehmigung durch Health Canada. Es hat einen Wert von etwa 690 Millionen US-Dollar (kanadische Dollar), berechnet auf 530 US-Dollar pro Kurs und einem Wechselkurs von 1,3 (ein „Kurs“ ist die Gesamtzahl der Dosen, die erforderlich sind, um ein Behandlungsschema abzuschließen.)
(Gemäß derselben Ankündigung hat die kanadische Regierung auch einen Vertrag zum Kauf von Mercks Covid-Medikament Molnupiravir für 500.000 Kurse unterzeichnet, und die Option zum Kauf weiterer 500.000 Kurse wartet auf die Genehmigung durch Health Canada.) ( Molnupiravir wurde von der US-amerikanischen FDA zugelassen am 23. Dezember 2021 kurz danach, trotz ernsthafter Bedenken . Molnupiravir ist weniger wirksam , giftiger und schwangere Frauen. Trotz ernsthafter Bedenken, dass die Einnahme ein Kind mit angeborener Behinderung zur Welt bringen könnte, wurde es am 23. Dezember von der US-Zulassungsbehörde FDA zugelassen , kurz danach 2021. Die FDA ist 18 Jahre alt. Zugelassen für den Verkauf an „Hochrisiko“-Personen mit diesen leichten bis mittelschweren Covids, die positiv getestet werden und schwere Covid entwickeln. Health Canada hat es noch nicht zugelassen . , Das andere berichten die Medien Länder sind auch beim Verkauf dieses Medikaments vorsichtig . )Es gibt noch mehr. Beispielsweise wurde Nilmatrelvir/Ritonavir bei keinem geimpften oder zuvor entwickelten COVID getestet. Trotzdem sind sie eine der ersten Personen, die die Behörden wollen.
Es wurde überhaupt nicht an schwangeren oder stillenden Frauen getestet.
Pfizer erklärt auf Seite 12 der Produktmonographie , dass Paxlobid „nicht bei schwangeren Frauen angewendet werden sollte, es sei denn, der potenzielle Nutzen überwiegt die potenziellen Risiken für den Fötus.“ Das tue ich.
Es gibt jedoch keine derartigen Warnhinweise bezüglich der Anwendung von Nilmatrelvir/Ritonavir durch stillende Frauen.Wie am Anfang dieses Artikels erwähnt, besteht eine Einzeldosis Paxroid aus 2 Tabletten Nermaltrelvir und 1 Tablette Ritonavir. Ein Satz von 3 Tabletten sollte innerhalb von 5 Tagen nach Auftreten der Symptome und zweimal täglich für 5 Tage eingenommen werden.
Ritonavir wird seit 1996 von Menschen mit HIV angewendet. Es ist allgemein bekannt, dass Ritonavir schwerwiegende, lebensbedrohliche Symptome wie Pankreatitis, Myokardinfarkt, Leberschäden, schwere Hautausschläge und allergische Reaktionen verursacht.
Nirmatrelvir /Ritonavir wurde jedoch nicht bei Patienten mit Leberfunktionsstörungen untersucht. Darüber hinaus warnen Pfizer und Regierungsbeamte beispielsweise diejenigen, bei denen das Risiko einer Leberfunktionsstörung besteht (z. B. Personen, die Hepatitis B oder C hatten, Personen mit hohen Leberfunktionstestergebnissen usw.). Wir warnen Sie nicht dass Sie Nirmatrelville/Ritonavir nicht einnehmen sollten.
Im Gegenteil, es stellt die benachteiligten Menschen, wie die Schwachen, die Alten und die Armen, in den Vordergrund.
Laut einem Artikel der CBC News vom 25. Januar sagte beispielsweise Howard Nijo, stellvertretender Beamter für öffentliche Gesundheit in Kanada: „Menschen mit geschwächter Immunität, Menschen über 80, geografisch oder sozioökonomisch. Menschen, die aufgrund von Problemen keine medizinische Versorgung erhalten können, sollten dies tun erhalten das Medikament zuerst, unabhängig davon, ob sie geimpft sind oder nicht .
Quebec ist einer der ersten Orte, an dem dieser Impfstoff für diese gefährdeten Personen eingesetzt wird. Bis März erhalten Sie genug Medikamente, um mehr als 25.000 Menschen zu behandeln. Dazu gehören Menschen mit „schweren Erkrankungen, die nicht geimpft werden können“. Danach sagt er, er werde die Leitung für andere öffnen.
Daher scheinen Politiker, Regierungsbeamte und Pfizer die Nachfrage auf die gleiche Weise anzuheizen wie bei Impfstoffen.
Zunächst haben wir eine relativ kleine Anzahl von Medikamenten.
Auch große Medien machen die Droge hoch. Zum Beispiel berichtete der Montrealer Journalist Verity Stephenson am 18. Januar CBC, dass „ Paxrovid das Risiko einer Krankenhauseinweisung und des Todes um 89 % im Vergleich zu Placebo reduziert hat.“ das Medikament als „Placebo“-Medikament bezeichnet wurde für sein Potenzial gelobt, Krankenhausaufenthalte wegen Viren zu reduzieren.“
Als Beispiel für einen insgesamt sehr positiven Bericht ist hier ein Artikel, der heute im Toronto Star veröffentlicht wurde.
Der Artikel der National Post vom 25. Januar 2022 ist etwas außergewöhnlich. Der Autor Tom Blackwell weist auf das Problem hin, dass Paxlobid die Wirkung anderer Medikamente stört (dazu später mehr). Tom Blackwell weist auf das Problem hin, dass Paxlobid die Wirkung anderer Arzneimittel beeinträchtigt, erwähnt jedoch kaum die Hauptnachteile anderer Arzneimittel.Doch selbst die Bundesregierung von Kanada sagte auf einer öffentlichen Webseite über Pillen : „Nicht viele Menschen haben Paxrovid eingenommen. Es können schwerwiegende und unerwartete Nebenwirkungen auftreten. Paxrovid wird noch untersucht, daher wissen Sie zu diesem Zeitpunkt möglicherweise nicht alles die Nebenwirkungen.
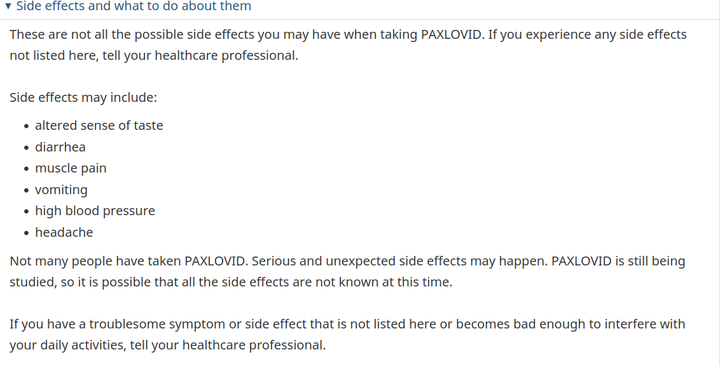
Weiter unten auf derselben Seite heißt es, alle vermuteten Nebenwirkungen direkt an Health Canada zu melden.
Leider ist es jedoch unwahrscheinlich, dass die Bundesregierung all diese Berichte getreu zusammenfasst und veröffentlicht, beispielsweise aufgrund der erheblich zu wenig berichteten schwerwiegenden Folgen und Todesfälle des COVID-Impfstoffs.
Im Rahmen der EUA hat die FDA Pfizer aufgefordert , „schwerwiegende unerwünschte Ereignisse und alle Medikationsfehler im Zusammenhang mit der Anwendung von Paxlobid “ zu melden . Darüber hinaus sind Gesundheitseinrichtungen und medizinisches Fachpersonal, die Paxrovid erhalten, verpflichtet, schwerwiegende unerwünschte Ereignisse und Medikationsfehler zu verfolgen und zu melden. Es ist jedoch wiederum höchst unwahrscheinlich, dass es sich um einen vollständigen und ehrlichen öffentlichen Bericht handelt.
(Die FDA forderte außerdem, dass der FDA bis zum Ende der Studie im April weitere Testergebnisse zur Sicherheit und Wirksamkeit zur Verfügung gestellt werden.)
Es gibt also nicht einmal vor, sicher und effektiv zu sein.Außerdem möchte ich drei der verschiedenen Probleme rund um Paxrovid vorstellen.
1. Die US-Zulassungsbehörde FDA hat den wichtigen Schritt ausgelassen, die Meinung des Beratungsgremiums anzuhören, bevor sie eine Notfallzulassung für Paxlovid erteilt.
Das Komitee heißt „Antibacterial Drug Advisory Board“. Mitglieder dieses Ausschusses prüfen Daten zu Arzneimitteln, für die Pharmaunternehmen eine Zulassung beantragen. Die Sitzungen des Komitees sind öffentlich und die Medien und andere werden daran teilnehmen.
Andererseits wurde es im Fall von Molnupiravir Ende November 2021 einberufen, wobei die Mitglieder mit 13:10 abstimmten und am 23. Dezember 2021 von der FDA genehmigt wurden.Ich wusste das, weil ich zufällig einen Artikel über Paxlobid fand, der am 6. Januar 2022 auf SonsOfLibertyMedia.com veröffentlicht wurde. Dieser Artikel präsentiert den Bloomberg Law-Artikel vom 22. Dezember 2021 über die Kontroverse, die durch das Überspringen dieses wichtigen Schritts durch die FDA verursacht wurde, aus einer Fülle aufschlussreicher Informationen .
Podiumssitzungen werden normalerweise nur mit Stempeln abgestempelt, aber dennoch werden sie sehr selten ausgelassen. 2. Ritonavir ist nicht nur ein Proteasehemmer, sondern reduziert auch die Aktivität eines sehr wichtigen Enzyms namens CYP3A4. CYP3A4 wird in der Leber produziert. CYP3A4 wird in der Leber produziert und spielt eine zentrale Rolle bei der Metabolisierung (Abbau) vieler Medikamente und Toxine. Dies ist notwendig, bevor Medikamente und Giftstoffe aus dem Körper ausgeschieden werden.
Ritonavir (und damit Paxrovid) reduziert die Aktivität von CYP3A4, wodurch große Mengen von Medikamenten und Toxinen länger im Körper verbleiben können.
Die Website der kanadischen Bundesregierung zu Paxrovid bestätigt , dass „viele Medikamente mit Paxrovid interagieren “ . „Die Einnahme von Paxrovid zusammen mit diesen Arzneimitteln kann schwerwiegende oder lebensbedrohliche Nebenwirkungen haben“ , räumt er ein.
Es gibt mehr als 100 Arzneimittel, deren Einnahme zusammen mit Paxrovid Pfizer Ihnen nicht gestattet . Einige von ihnen sind sehr weit verbreitet, wie Lidocain, Warfarin, Phenobarbital, Erythromycin, Johanniskraut, Fentanyl, Methadon, Midazolam und Prednison.
- 3. Die in der Pressemitteilung von Pfizer Inc. aus den Vereinigten Staaten vom 5. November 2021 enthaltenen Studienergebnisse basieren auf der statistischen Analyse „ Therapeutic Intent“. Diese sind überhaupt nicht streng.
Betrachtet man die Bedeutung von „Behandlungsabsicht“ , so zeigt sich, dass dieser auf der Annahme beruht, dass die Studienteilnehmer behandelt wurden, unabhängig davon, ob sie tatsächlich behandelt wurden oder nicht. Viele Veröffentlichungen zu diesem Ansatz beteuern, dass er solide ist. Aber objektiv ist es ganz anders. (Ich habe vor mindestens 20 Jahren begonnen, die Analyse der Behandlungsabsicht in der medizinischen Forschung zu bemerken, die, soweit ich weiß, vermeiden soll, ehrlich über die Wirkung und Wirksamkeit des untersuchten Medikaments zu berichten. Methode, und immer noch so
Und um auf der sicheren Seite zu sein, verwendet die Pressemitteilungsstudie von Pfizer nicht nur das, sondern ihre Analyse der therapeutischen Absicht verwendet einen „korrigierten“ Ansatz. Insbesondere umfasst dies beispielsweise Personen, die zu Beginn der COVID-19-Behandlung keine mAb-Therapie (monoklonale Antikörper) erhalten haben oder voraussichtlich erhalten werden.
Das ist nicht möglich.
Ich hoffe aufrichtig, dass die Mitarbeiter, die den Druck zurückdrängen, Paxrovid vielen Menschen zu verabreichen, definitiv gewinnen werden.

0 Comments